Chemische Verbindungen mit den Elementen C, H & O sind die essentielle Basis für die organische Chemieindustrie. Die in natürlichen Ressourcen vorkommenden C- , H- & O-Verbindungen sind sehr komplex. Für die chemische Produktion müssen sie in geeignete Moleküle umgewandelt werden. Das erfolgt in der Regel in thermischchemischen Umwandlungsprozessen bei hohen Temperaturen und häufig auch bei hohen Drücken.
Thermisch-chemische Umwandlung durch Pyrolyse
Pyrolyse ist die thermische Zersetzung bei erhöhten Temperaturen unter Luftabschluss. Pyrolyseprozesse finden bei Temperaturen zwischen 150 – 1100 °C statt. Durch Pyrolyse werden z.B. Steinkohlenkoks für die Eisen- und Stahlherstellung im Hochofen sowie Holzkohle zum Grillen hergestellt.
Thermisch-chemische Umwandlung durch Gasifizierung
Gasifizierung ist die thermisch-chemische Umwandlung zu Gasen, hauptsächlich Kohlenstoffmonoxid (CO) und Wasserstoff (H₂), bei hohen Temperaturen. Gasifizierungsprozesse finden bei Temperaturen über 800 °C statt. Sauerstoff (O₂) wird benötigt, um diese hohen Temperaturen zu erreichen. Häufig braucht man zusätzlich auch Wasserdampf (H₂O).
Synthesegas – auch Syngas genannt – besteht hauptsächlich aus Kohlenstoffmonoxid (CO) und Wasserstoff (H₂). Aus Syngas lassen sich viele Basischemikalien wie Methanol, Ammoniak oder Paraffine herstellen. Mögliche Folgeprodukte sind Kunststoffe, Düngemittel oder auch hochwertige CO₂-reduzierte bzw. CO₂-neutrale synthetische Kraftstoffe (Kerosin, Diesel und Benzin).

Wusstest du, wie …
... sich Verbrennung und Gasifizierung unterscheiden? Wir erklären es am Einsatzstoff Abfall.

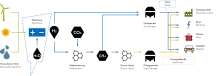
Chemische Produkte können auch aus Kohlenstoffdioxid (CO₂) und Wasserstoff (H₂) erzeugt werden - allein durch die Zufuhr von Strom. Dies wird Power-to-X (PtX) genannt. Die Vorteile von PtX sind, dass CO₂ und H₂ nahezu unbegrenzt vorhanden sind und fluktuierender erneuerbarer Strom langfristig speicherbar wird
Power-to-X (PtX)
... ist die Herstellung von chemischen Produkten (X) aus Strom. Mit Strom wird Kohlenstoffdioxid (CO₂) aus Abgasen oder aus der Luft abgetrennt und Wasserstoff (H₂) durch Elektrolyse aus Wasser (H₂O) gewonnen. Als Syntheseprodukte aus diesen beiden Gasen können viele Basischemikalien wie Methanol und Paraffine hergestellt werden. Mögliche Folgeprodukte sind Kunststoffe oder CO₂-neutrale synthetische Kraftstoffe wie Kerosin, Diesel und Benzin.¹
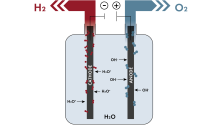
Wasserelektrolyse
... ist die Spaltung von Wasser in H₂ und O₂ durch Strom. Eine CO₂-neutrale, umweltfreundliche Wasserelektrolyse wird mit regenerativ erzeugtem Strom betrieben. Dabei entsteht CO₂-neutraler „grüner“ Wasserstoff. Er kann in Brennstoffzellen für die Mobilität, für die Strom- und Wärmeerzeugung oder als Reaktionsgas in der Chemie und in der Metallurgie genutzt werden. Der Nachteil ist, dass die Wasserelektrolyse sehr viel Strom benötigt.